初中化學(xué)整本書的“知識框架圖”,讓孩子完美逆襲!(建議收藏)
提示您本文原始標(biāo)題是:初中化學(xué)整本書的“知識框架圖” , 讓孩子完美逆襲!(建議收藏)
第一單元:走進化學(xué)世界
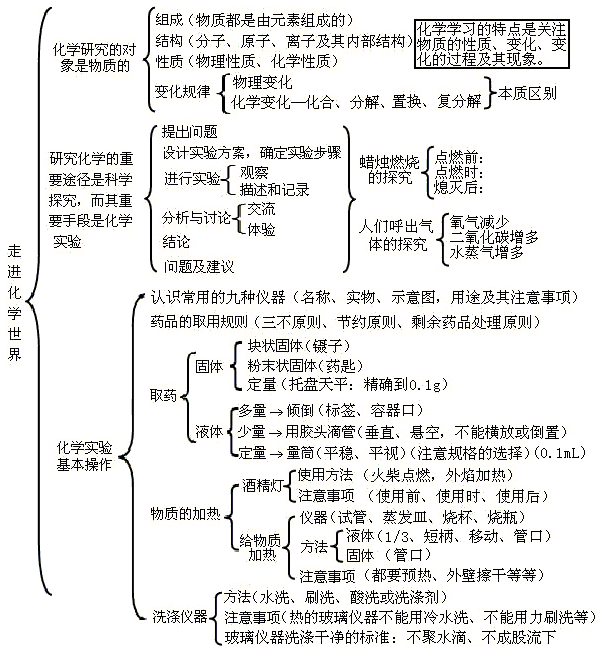
---- 初中化學(xué)整本書的“知識框架圖” , 讓孩子完美逆襲!(建議收藏) //---- http:// //
第二單元:我們周圍的空氣
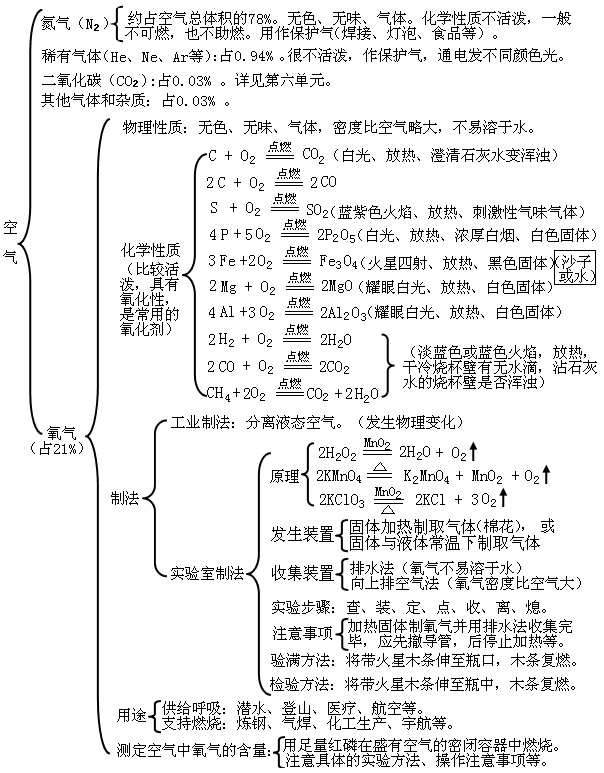
---- 初中化學(xué)整本書的“知識框架圖” , 讓孩子完美逆襲!(建議收藏) //---- http:// //
第三單元:自然界的水
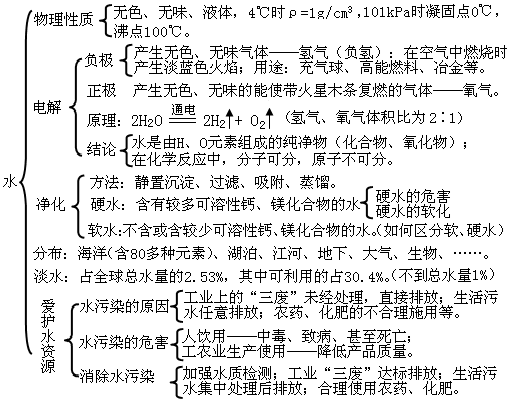
---- 初中化學(xué)整本書的“知識框架圖” , 讓孩子完美逆襲!(建議收藏) //---- http:// //
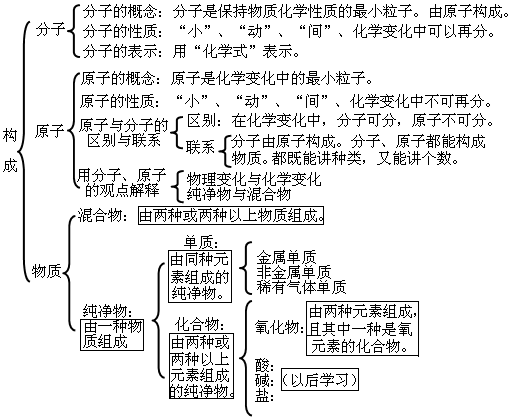
---- 初中化學(xué)整本書的“知識框架圖” , 讓孩子完美逆襲!(建議收藏) //---- http:// //
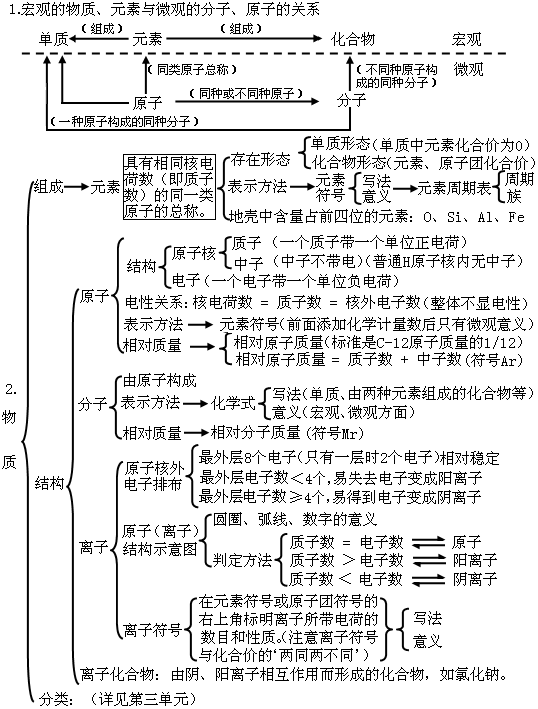
第四單元:物質(zhì)構(gòu)成的奧秘
---- 初中化學(xué)整本書的“知識框架圖” , 讓孩子完美逆襲!(建議收藏) //---- http:// //
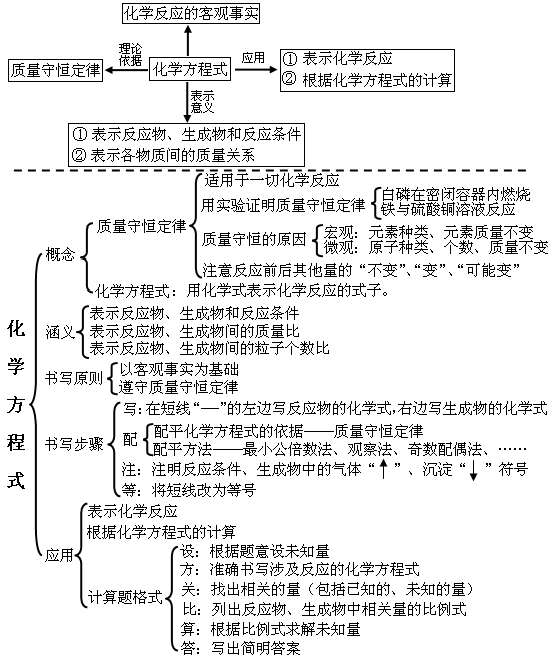
第五單元:化學(xué)方程式
---- 初中化學(xué)整本書的“知識框架圖” , 讓孩子完美逆襲!(建議收藏) //---- http:// //
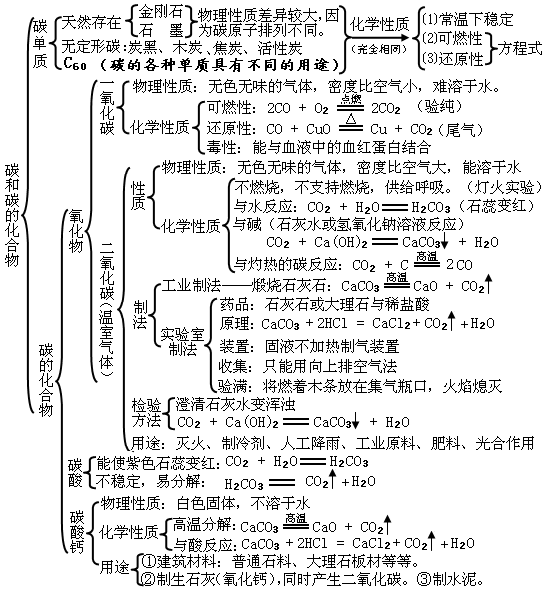
第六單元:碳和碳的氧化物
---- 初中化學(xué)整本書的“知識框架圖” , 讓孩子完美逆襲!(建議收藏) //---- http:// //
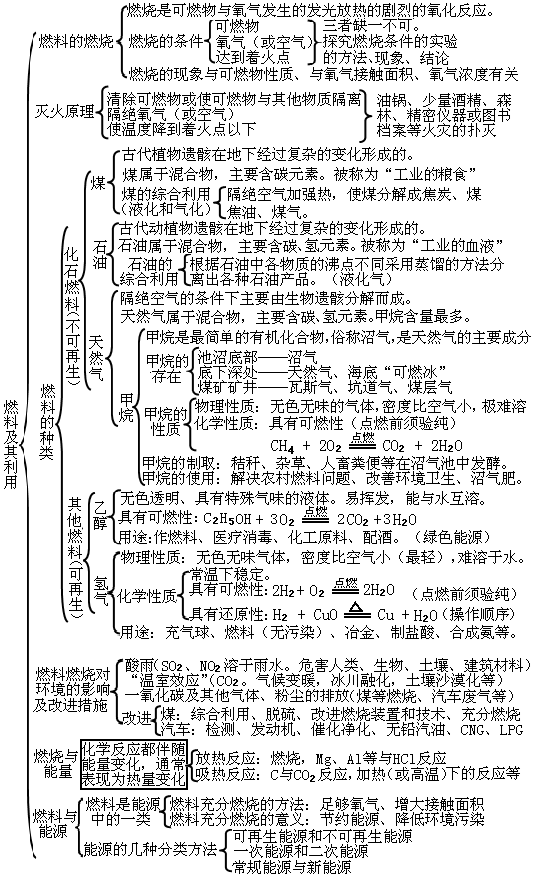
第七單元:燃料及其利用
---- 初中化學(xué)整本書的“知識框架圖” , 讓孩子完美逆襲!(建議收藏) //---- http:// //
第八單元:金屬和金屬材料
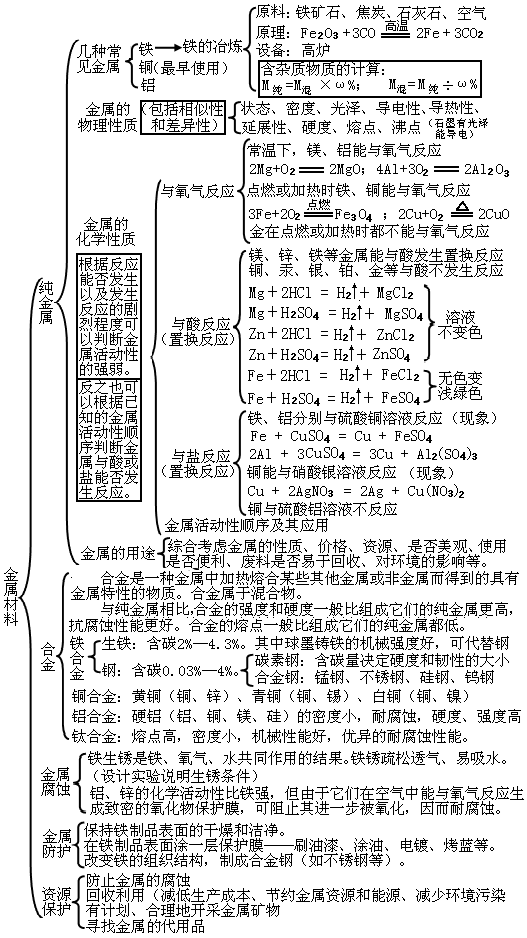
---- 初中化學(xué)整本書的“知識框架圖” , 讓孩子完美逆襲!(建議收藏) //---- http:// //
第九單元:溶液
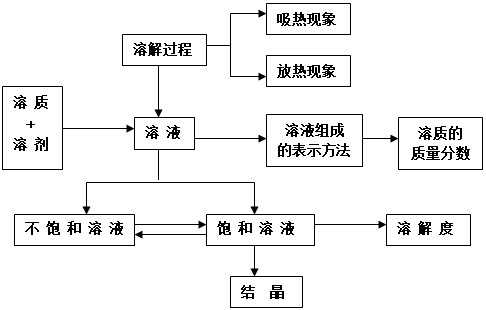
---- 初中化學(xué)整本書的“知識框架圖” , 讓孩子完美逆襲!(建議收藏) //---- http:// //
第十單元:酸 堿 鹽
1
化學(xué)用語
1、電離方程式:
2、物質(zhì)的俗稱和主要成分:
生石灰CaO;
熟石灰、消石灰、石灰水的主要成分Ca(OH)2;
石灰石、大理石CaCO3;
食鹽的主要成分NaCl ;
純堿、口堿Na2CO3;
燒堿、火堿、苛性鈉NaOH;
膽礬、藍(lán)礬CuSO4·5H2O;
碳酸鈉晶體Na2CO3.10H2O;
氨水NH3.H2O 。
2
金屬活動性
1、金屬活動性順序:
K>Ca>Na>Mg>Al>Zn>Fe>Sn>Pb(H)Cu>Hg>Ag>Pt>Au
2、金屬活動性順序的意義:
在金屬活動性順序中 , 金屬位置越靠前 , 金屬在水溶液(酸溶液或鹽溶液)中就越容易失電子而變成離子 , 它的活動性就越強 。
3、金屬活動性順序的應(yīng)用:
(1)排在氫前的金屬能置換出酸里的氫(元素) 。
(2)排在前面的金屬才能把排在后面的金屬從它們的鹽溶液中置換出來(K、Ca、Na除外) 。
3
酸、堿、鹽的溶解性
1、常見鹽與堿的溶解性:
鉀(鹽)、鈉(鹽)、銨鹽全都溶 , 硝酸鹽遇水影無蹤 。
硫酸鹽不溶硫酸鋇 , 氯化物不溶氯化銀 。
碳酸鹽只溶鉀(鹽)、鈉(鹽)、銨(鹽) 。
堿類物質(zhì)溶解性:只有(氫氧化)鉀、(氫氧化)鈉、(氫氧化)鈣、(氫氧化)鋇溶 。
2、八個常見的沉淀物:
氯化銀、硫酸鋇碳酸銀、碳酸鋇、碳酸鈣、氫氧化鎂、氫氧化銅、氫氧化鐵
3、四微溶物:
Ca(OH)2(石灰水注明“澄清”的原因)、
CaSO4(實驗室制二氧化碳時不用稀硫酸的原因)
Ag2SO4(鑒別SO42-和Cl-時 , 不用硝酸銀的原因)、
MgCO3(碳酸根離子不能用于在溶液中除去鎂離子的原因)
4、三個不存在的物質(zhì):
氫氧化銀、碳酸鋁、碳酸鐵
4
復(fù)分解反應(yīng)發(fā)生的條件反應(yīng)
有氣體、水或沉淀生成(即有不在溶液中存在或在水溶液中不易電離的物質(zhì))
1、不溶性堿只能與酸性發(fā)生中和反應(yīng);
2、不溶性鹽 , 只有碳酸鹽能與酸反應(yīng);
3、KNO3、NaNO3、Agcl、BaSO4不能做復(fù)分解反應(yīng)的反應(yīng)物 。
5
溶液的酸堿性與酸堿度的測定
1、指示劑---溶液的酸堿性紫色的石蕊試液遇酸性溶液變紅;遇堿性溶液變藍(lán)
無色的酚酞試液只遇堿溶液變紅
注:不溶性堿與指示劑無作用;
堿性溶液不一定是堿的溶液(特例:碳酸鈉的水溶液顯堿性)
2、pH值---溶液的酸堿度:
pH<7溶液為酸性(越小酸性越強);
pH=7溶液為中性;
pH>7溶液為堿性(越大堿性越強)
6
離子的檢驗
Cl-(在溶液中)---在被測溶液中加入硝酸銀溶液,如果生成不溶于硝酸的白色沉淀 , 則原被測液中含氯離子 。
SO42-(在溶液中)---在被測溶液中加入氯化鋇(或硝酸鋇、或氫氧化鋇)溶液 , 如果生成不溶于硝酸(或鹽酸)的白色沉淀 , 則原被測液中含硫酸根離子 。
CO32-
(1)(固體或溶液)---在被測物質(zhì)中加入稀酸溶液 , 如果產(chǎn)生能使澄清石灰水變渾濁的氣體 , 則原被測物質(zhì)中含碳酸根離子 。
(2)(在溶液中)---在被測溶液中加入氯化鋇或硝酸銀溶液 , 如果產(chǎn)生能溶于硝酸的白色沉淀 , 且同時生成能使澄清的石灰水變渾濁的氣體 , 則原被測溶液中含碳酸根離子 。
1、在鑒別Cl-和SO42-時 , 用氯化鋇溶液 , 不要用硝酸銀溶液 , 這是因為硫酸銀為微溶性物質(zhì) , 使鑒別現(xiàn)象不明顯;
2、在一未知溶液中加入氯化鋇溶液 , 若產(chǎn)生不溶于硝酸的白色沉淀 , 則原被測液中可能含銀離子也可能含硫酸根離子 。 )
7
物質(zhì)的顏色
1、固體(多為白色)
黑色---CuO、C粉、MnO、2Fe3O4、
紫黑色---KMnO4
紅色---Cu、Fe2O3
紅褐色---Fe(OH)3
藍(lán)色---Cu(OH)2、CuSO4.5H2O 綠色---Cu2(OH)2CO3
2、溶液(多為無色)
淺綠色溶液---(亞鐵鹽溶液)FeCl2溶液、FeSO4;
黃色溶液--- (鐵鹽溶液)FeCl3溶液、Fe2(SO4)3 溶液、Fe(NO3)3;
溶液藍(lán)色溶液---(銅鹽溶液)CuCl2溶液、CuSO4溶液、Cu(NO3)2;
溶液藍(lán)綠色溶液-CuCl2溶液(較濃) 。
8
酸、堿、鹽的特性
1、濃鹽酸---有揮發(fā)性、有刺激性氣味、在空氣中能形成酸霧 。
2、濃硝酸---有揮發(fā)性、有刺激性氣味、在空氣中能形成酸霧 , 有強氧化性 。
3、濃硫酸---無揮發(fā)性 。 粘稠的油狀液體 。 有很強的吸水性和脫水性 , 溶水時能放出大量的熱 。 有強氧化性 。
4、氫氧化鈣---白色粉末、微溶于水 。
5、氫氧化鈉---白色固體、易潮解 , 溶水時放大量熱 。 能與空氣中的二氧化碳反應(yīng)而變質(zhì) 。
6、硫酸銅---白色粉末、溶于水后得藍(lán)色溶液(從該溶液中析出的藍(lán)色晶體為五水合硫酸銅CuSO4.5H2O) 。
7、碳酸鈉---白色粉末 , 水溶液為堿性溶液(從溶液中析出的白色晶體為碳酸鈉晶體Na2CO3.10H2O) 。
8、氨水(NH3.H2O)---屬于堿的溶液 。
9
酸與堿的通性和鹽的性質(zhì)
1、酸的通性
(1)酸溶液能使紫色的石蕊試液變紅 , 不能使無色的酚酞試液變色;
(2)酸能與活潑金屬反應(yīng)生成鹽和氫氣;
(3)酸能與堿性氧化物反應(yīng)生成鹽和水;
(4)酸能與堿反應(yīng)生成鹽和水;
(5)酸能與某些鹽反應(yīng)生成新的鹽和新的酸 。
2、堿的通性
(1)堿溶液能使紫色的石蕊試液變藍(lán) , 并能使無色的酚酞試液變紅色;
(2)堿能與酸性氧化物反應(yīng)生成鹽和水;
(3)堿能與酸反應(yīng)生成鹽和水;
(4)某些堿能與某些鹽反應(yīng)生成新的鹽和新的堿 。
3、鹽的性質(zhì)
(1)某些鹽能與較活潑的金屬反應(yīng)生成新的鹽和金屬;
(2)某些鹽能與酸反應(yīng)生成新的鹽和新的酸;
(3)某些鹽能與某些堿反應(yīng)生成新的鹽和新的堿 。
- 「女性之音」初中女生“停止發(fā)育”的3大信號,別不當(dāng)回事,或是身高止步155
- 現(xiàn)代金報■寧波兒保醫(yī)生寫的這本書火了!15萬字干貨,都是家長們問的最多的…
- 『西紅柿媽咪』原創(chuàng)為何00后才讀初中,身高就動不動一米八?因為他們有這四大優(yōu)勢
- 初中男生不再“長高”的3個跡象,中2個的話,身高可能定型了!
- 初中生一旦得了“抑郁癥”,會常把這3句話掛嘴邊,不妨自檢
- 書單來了丨5本書教孩子堅持做自己,不盲從、更自信
- 初中女生身高還是150?趁早改掉這3個“壞習(xí)慣”,再猛躥一把
- 初中女生身高不到165?這3件事可就別再做了,不然會影響長高
- 聰明的孩子是如何學(xué)習(xí)的 | 孩子成績差一定在作妖?
- 初中生軍訓(xùn),列隊時身高差懸殊,孩子是真矮還是晚長?
